 Sağlık
Sağlık
 Sağlık
Sağlık
 Otomobil
Otomobil
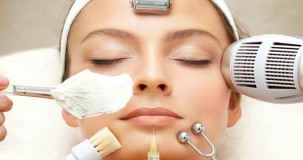 Moda ve Güzellik
Moda ve Güzellik
 Kültür ve Sanat
Kültür ve Sanat
 Faydalı Bilgiler
Faydalı Bilgiler
 Eğitim
Eğitim
 Doğa ve Hayvanlar
Doğa ve Hayvanlar
CO (karbonmonoksit) bileşiği , bir karbon atomu ile bir oksijen atomunun birleşmesiyle oluşur. Bu bileşikte karbon ve oksijen arasında üçlü bağ bulunur
CO bileşiğinin oluşumuyla ilgili bazı örnekler:
CO bileşiği, renksiz, kokusuz ve tatsız bir gazdır. Bu nedenle "sessiz katil" olarak adlandırılır
Karbon monoksit bileşiğinin formülü CO'dur.
CO (karbon monoksit), organik bir bileşik değildir çünkü karbon ve hidrojen atomları arasında karbon-hidrojen bağları bulunmaz. Ayrıca, CO, CO2, Na2CO3 ve KCN gibi karbon içeren bazı bileşikler, karbon atomlarının bağlanma şekli nedeniyle organik olarak sınıflandırılmaz.
CO (karbon monoksit) ve CO2 (karbondioksit) arasındaki temel farklar şunlardır: Kimyasal Bileşim: CO, bir karbon ve bir oksijen atomundan (CO), CO2 ise bir karbon ve iki oksijen atomundan (CO₂) oluşur. Doğal Oluşum: CO2, doğal olarak atmosferde bulunur ve solunum ile volkanik aktiviteler gibi doğal süreçlerle oluşur. Sağlık Üzerindeki Etkiler: CO, solunduğunda kandaki hemoglobine bağlanarak oksijen taşıma yeteneğini azaltır ve zehirlenmeye yol açabilir. Çevresel Etki: CO2, sera gazı olarak iklim değişikliğine katkıda bulunur. Flammability (Yanıcılık): CO yanıcı bir gazdır, CO2 ise yanıcı değildir.
Bir bileşiğin formülü, bileşikteki elementlerin atom sayılarının oranını gösteren basit formül veya bileşik içindeki atomların gerçek sayılarını gösteren molekül formülü ile ifade edilebilir. Basit formül. Molekül formülü. Bir bileşiğin formülünü bulmak için şu adımlar izlenebilir: 1. Elementlerin mol sayısının belirlenmesi. 2. Mol sayılarının en küçük tam sayıya bölünmesi. 3. Formülün yazılması. Bileşik formüllerinin bulunması için kimyasal hesaplamalar ve elementlerin değerliklerinin bilinmesi gerekebilir.
 Eğitim
Eğitim
Boğaziçi Fen Edebiyat Fakültesi hangi kampüste?
Canlının genetik yapısı nasıl belirlenir?
Chimera insan ne demek?
Bir fonksiyonun türevi varsa birebirdir ne demek?
CO bileşiği nasıl oluşur?
Cosmos Yeni Dünyalar ne anlatıyor?
Biyolojik tehlike işareti aşağıdakilerden hangisidir?
Bursa'da okullar ne zaman tatil?
Biyolog ve doktor arasındaki fark nedir?
Boylamsal araştırma nedir?